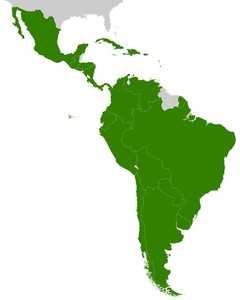
AMLAC, un organismo regional para América Latina y el Caribe, se está creando para promover un mayor acceso a equipos médicos y medicamentos seguros y eficaces mediante una combinación de normativas regionales.
El 26 de abril de 2023, titulares de las agencias sanitarias de Colombia, Cuba y México, y más concretamente, el Instituto Nacional de Vigilancia de Medicamentos y Alimentos (INVIMA) de Colombia, el Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos (CECMED) de Cuba y la Comisión Federal para la Protección contra Riesgos Sanitarios (COFEPRIS) de México firmaron la Declaración de Acapulco para la creación de la Agencia Reguladora de Medicamentos y Dispositivos Médicos de Latinoamérica y el Caribe, AMLAC.
La declaración reconoce los desafíos que enfrentan América Latina y El Caribe en los ámbitos sanitario, productivo, económico y social, especialmente en momentos de emergencia como la pandemia de COVID-19, la cual reveló en su momento las desigualdades sanitarias y atención médica que imperan en la región ante una emergencia de tal magnitud.
El Ministro de Asuntos Exteriores de Cuba declaró que: ‘La creación de la AMLAC busca lograr la autosuficiencia sanitaria de América Latina y el Caribe’. La Agencia será un mecanismo ‘para contribuir a la integración regional a través de la armonización y la convergencia en la regulación sanitaria, en favor del acceso a medicamentos y dispositivos médicos seguros, eficaces y de calidad’.
El objetivo de AMLAC es unir esfuerzos por la seguridad sanitaria de América Latina y para hacer frente a las emergencias en materia de salud, en particular cuando existe un contexto de inequidad sistémica que se vuelve alarmante cuando se trata del acceso a insumos de la salud, según señaló el titular de la Comisión Federal para la Protección contra Riesgos Sanitarios (COFEPRIS).
La Declaración fue firmada por representantes de los organismos reguladores de control y vigilancia de salud de los países firmantes: Alejandro Svarch, titular de COFEPRIS en México, Mariela Pardo, quien está al frente de INVIMA en Colombia y por Olga Lidia Jacobo Casanueva, la directora del CECMED en Cuba.
También estuvieron presentes a la firma de la Declaración los embajadores de Colombia, Cuba y Honduras, así como el coordinador de la presidencia pro-tempore de la Comunidad de Estados Latinoamericanos y Caribeños (PPT-CELAC), entre otros.
Los titulares de las agencias sanitarias de Colombia, Cuba y México establecieron el compromiso de informar y presentar los avances de sus trabajos ante la CELAC, donde surgió la iniciativa en enero de 2023.
En la actualidad, 10 países se han sumado a este nuevo mecanismo de cooperación regional, mientras que Argentina, Brasil y Chile han declinado hasta ahora adherirse. Las últimas reuniones presenciales se llevaron a cabo en mayo de 2023 en Bogotá, Colombia, y la próxima se llevará a cabo en junio de 2023 en La Habana, Cuba.
El desarrollo de los productos biológicos y biotecnológicos en América Latina es muy diverso debido a las particularidades relativas a numerosos factores tales como factores culturales, económicos, políticos y regulatorios. Cada país latinoamericano posee por lo tanto un mercado y un panorama regulatorio únicos [1].
La actual creación de AMLAC ayudará en definitiva a fortalecer los mecanismos para la armonización y el reconocimiento de las regulaciones, para lograr que el registro de un medicamento o dispositivo médico aprobado por la agencia sea reconocido por el resto de los países miembros.
Artículos relacionados
Escenario regulatorio sobre productos bioterapéuticos similares en Latinoamérica
Colaboración entre autoridades reguladoras sobre biosimilares
|
FORO LATINOAMERICANO
Se ha lanzado la nueva sección del ‘Foro Latinoamericano’ sobre GaBI. El objetivo de esta nueva sección es brindarle las últimas noticias y actualizaciones sobre desarrollos de medicamentos genéricos y biosimilares en América Latina en español. Ver el último artículo de cabecera: AMLAC: agencia reguladora de medicamentos de América Latina y el Caribe establecida !Explore las noticias en el Foro Latinoamericano! Regístrese para recibir el boletín informativo GaBI Foro Latinoamericano. Informe a colegas y amigos sobre esta nueva iniciativa.
|
Referencia
1. GaBI Online - Generics and Biosimilars Initiative. Regulación del registro de medicamentos biológicos en América Latina [www.gabionline.net]. Mol, Belgium: Pro Pharma Communications International; [cited 2023 Jun 12]. Available from: www.gabionline.net/es/biosimilares/investigacion/regulacion-del-registro-de-medicamentos-biologicos-en-america-latina
Permiso otorgado para reproducir solo para uso personal y no comercial. Cualquier otra reproducción, copia o reimpresión de todo o parte de cualquier "Contenido" que se encuentre en este sitio web está estrictamente prohibida sin el consentimiento previo del editor. Póngase en contacto con el editor para obtener permiso antes de redistribuir.
Copyright – a menos que se indique lo contrario, todo el contenido de este sitio web es © 2023 Pro Pharma Communications International. Todos los derechos reservados.








 0
0








Post your comment