El mercado farmaceútico brasileño ha experimentado muchos cambios desde que se introdujeron las leyes sobre medicamentos genéricos.
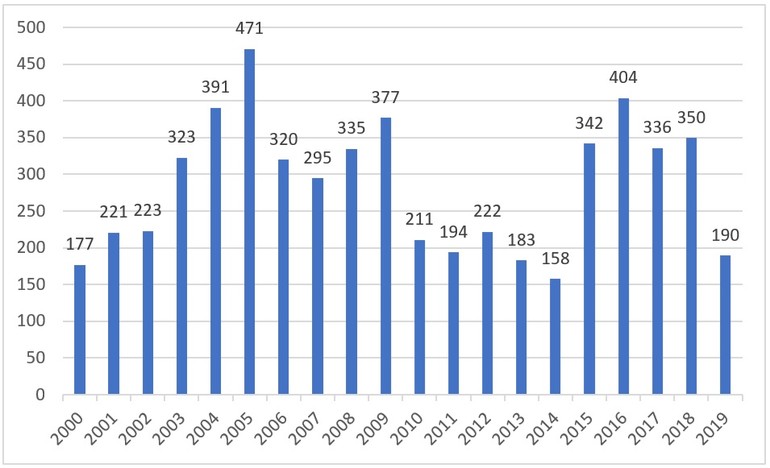
En 2000, la ANVISA (Agência Nacional de Vigilância Sanitária) aprobó la comercialización de 177 medicamentos genéricos en el mercado farmaceútico brasileño, ver Figura 1.
El mercado de medicamentos genéricos comenzó a crecer de manera constante, 19 años después de aprobarse los primeros, llegando a los 5,723 registros en 2019. En 19 años, se han cancelado 2,398 registros, dejando 3,325 registros de medicamentos genéricos válidos en agosto de 2019 [1].
En agosto de 2019, los tres principios activos con el mayor número de registros de medicamentos genéricos fueron la dipirona monohidrato (n = 46), amoxicilina (n = 40) y paracetamol (n = 37), los cuales juntos representan el 19.1% de todos los registros.
Figura 1: Número de medicamentos genéricos registrados por año, de 2000 a 2019
En 2017, los medicamentos genéricos representaron una pertinente representación del mercado farmaceútico en Brasil: 41% de las compañías, 37% de productos y 13.5% de ingresos. Aparte de ésto, en el mismo año, se vendieron más de 1.5 billones de medicamentos genéricos, volviéndose el medicamento más comercializado en el país. Aún así, en comparación con otros países, los medicamentos genéricos en Brasil siguen estando subrepresentados.
Comparado con otros países donde los medicamentos genéricos llevan más tiempo en el mercado, como Francia, Alemania y el Reino Unido, la representación de estos medicamentos es del 42%, 66% y 60%, respectivamente [1].
La concienciación del médico y de la población, junto con las limitaciones financieras han sido las razones por las que la demanda de medicamentos genéricos en Brasil ha ido en aumento. El aumento en el volumen de ventas ha resultado estar por encima del crecimiento de ingresos medio. Entre 2015 y 2017, los ingresos por medicamentos genéricos crecieron hasta un 28.3%, mientras que los ingresos por otros tipos de medicamentos crecieron una media de hasta un 5.6%.
Comentario del Editor
Lectores interesados en conocer más sobre políticas de genéricos en EE. UU. están invitados a visitar www.gabi-journal.net para ver el siguiente manuscrito en GaBI Journal:
Barriers to generics policy reform: a US case study
GaBI Journal está indexado en Embase, Scopus, Emerging Sources Citation Index y más.
Lectores interesados en contribuir con un artículo de investigación o perspectiva en español y/o inglés a GaBI Journal – una revista académica independiente, con revisión por pares – por favor envíe su manuscrito aquí.
Impacto de citación de GaBI Journal
1.9 - CiteScore 2020 (calculado el 5 de mayo de 2021)
1.7 - CiteScoreTracker 2021 (Última actualización el 4 de julio de 2021)
Envíe un manuscrito a GaBI Journal
Artículos relacionados
Leyes sobre el envasado, sustitución y prescripción de medicamentos genéricos en Brasil
Requisitos legales sobre estudios de equivalencia para medicamentos genéricos en Brasil
Backlog de patentes de medicamentos en Brasil
| Foro Latinoamericano Se ha lanzado la nueva sección del ‘Foro Latinoamericano’ sobre GaBI. El objetivo de esta nueva sección es brindarle las últimas noticias y actualizaciones sobre desarrollos de medicamentos genéricos y biosimilares en América Latina en español. Vea el artículo principal de esta semana: La MHRA del Reino Unido actualiza su directriz para conceder licencia de biosimilares Explore las noticias en el Foro Latinoamericano! Regístrese para recibir el boletín informativo GaBI Latin American Forum. Informe a colegas y amigos sobre esta nueva iniciativa.
|
Referencia
1. Nardi EP, Silva ARA. A closer look at generic drugs: the Brazilian case. In: Lowell T. Duncan (Ed). Advances in Health and Disease. Volume 21. Nova Science Publishers; 2020. Chapter 2. ISBN: 978-1-53617-783-1.
Permiso otorgado para reproducir solo para uso personal y no comercial. Cualquier otra reproducción, copia o reimpresión de todo o parte de cualquier "Contenido" que se encuentre en este sitio web está estrictamente prohibida sin el consentimiento previo del editor. Póngase en contacto con el editor para obtener permiso antes de redistribuir.
Copyright: a menos que se indique lo contrario, todo el contenido de este sitio web es © 2021 Pro Pharma Communications International. Todos los derechos reservados.








 0
0










Post your comment